Eine Brennstoffzelle ist ein elektrochemisches Gerät, das chemische Energie in Strom umwandelt. Es erzeugt ein Potential, indem es die Reaktionen trennt. Wasserstoff wird an der Anode oxidiert, während Sauerstoff an der Kathode reduziert wird. Derzeit befinden sich drei Haupttypen von Brennstoffzellen entweder in der Entwicklung oder in Betrieb. Jeder Typ bietet einzigartige Vorteile, Einschränkungen und Anwendungsmöglichkeiten. Die folgende Tabelle fasst die wichtigsten Merkmale dieser verschiedenen Brennstoffzellentypen zusammen:
| Brennstoffzellen-Typ | Betriebstemperatur | Kathodengas | Elektrolyt | Anodengas |
| Protonenaustauschmembran | 50-100 °C | Luft (Ø2 + N2) | Polymer (H+) | H2 |
| Alkalisch | 50-100 °C | Luft (Ø2 + N2) | KOH | H2 |
| Festes Oxid | 500-1000 °C | Luft (Ø2 + N2) | ZrO2 (Ø2-) | CH4, CO |
Brennstoffzellen mit Protonenaustauschmembran (PEM) #
Diese Brennstoffzellen verwenden ein festes Polymer als Elektrolyt und verfügen über poröse Kohlenstoffelektroden, in die ein Platinkatalysator eingebettet ist. Sie arbeiten nur mit Wasserstoff, Sauerstoff aus der Luft und Wasser, wodurch korrosive Flüssigkeiten überflüssig werden, die andere Brennstoffzellen möglicherweise benötigen. In der Regel werden diese Brennstoffzellen mit reinem Wasserstoff betrieben, der aus Lagertanks oder Reformern an Bord geliefert wird.
PEM-Brennstoffzellen funktionieren bei relativ niedrigen Temperaturen, etwa 50-100 °C. Der Platinkatalysator ist jedoch sehr anfällig für CO-Vergiftungen. Aus diesem Grund wird ein zusätzlicher Reaktor benötigt, um CO im Brenngas zu reduzieren, wenn der Wasserstoff aus Alkohol- oder Kohlenwasserstoffbrennstoffen stammt. Um dieses Problem anzugehen, untersuchen Entwickler Platin/Ruthenium-Katalysatoren, die eine größere Beständigkeit gegen CO aufweisen.
Transporation und stationäre Anwendungen verwenden häufig PEM-Brennstoffzellen. Strukturell besteht eine Protonenaustauschmembran-Brennstoffzelle aus einer Protonenaustauschmembran (Polymerelektrolyt), die zwischen einer Anode und einer Kathode positioniert ist. Die folgende Abbildung zeigt eine schematische Darstellung einer PEM-Brennstoffzelle.
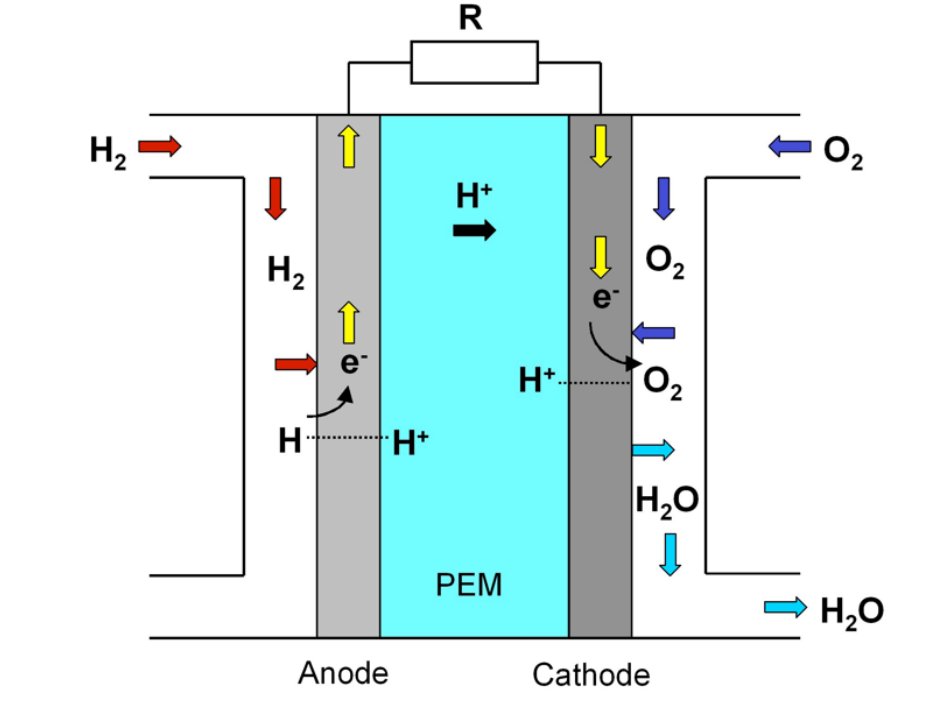
In der Brennstoffzelle laufen folgende Prozesse ab:
- Einführung von Wasserstoffbrennstoff: Wasserstoffbrennstoff wird durch Strömungsfeldplatten zur Anode auf einer Seite der Brennstoffzelle geleitet. Sauerstoff aus der Luft wird zur Kathode auf der gegenüberliegenden Seite geleitet.
- Sauerstoffreaktion an der Kathode: An der Kathode reagiert Sauerstoff mit den Protonen aus der Protonenaustauschmembran und den Elektronen aus der Elektrode.
- Wasserstoffdissoziation an der Anode: An der Anode dissoziieren und adsorbieren Wasserstoffmoleküle als Wasserstoffatome an einem Platinkatalysator.
- Protonentransfer: Die Protonenaustauschmembran lässt die positiv geladenen Wasserstoffionen zur Kathode gelangen.
Die Gesamtreaktion in der PEM-Brennstoffzelle ist: 2H2 + O2 → H2O.
Alkalische Brennstoffzellen #
Sie gehören zu den ersten Brennstoffzellentechnologien, die entwickelt wurden. Sie wurden im US-Raumfahrtprogramm häufig verwendet, um elektrische Energie und Wasser an Bord von Raumfahrzeugen zu erzeugen. Diese Brennstoffzellen verwenden eine Kaliumhydroxidlösung in Wasser als Elektrolyt. Sie können verschiedene Nichtedelmetalle als Katalysatoren an Anode und Kathode einsetzen.
Hochtemperatur-AFCs arbeiten bei Temperaturen zwischen 100 °C und 250 °C. Neuere Designs funktionieren bei niedrigeren Temperaturen von ca. 23 °C bis 70 °C. AFCs sind aufgrund der schnellen Geschwindigkeit chemischer Reaktionen innerhalb der Zelle Hochleistungs-Brennstoffzellen. Sie sind auch hocheffizient und erreichen Wirkungsgrade von 60 % in Raumfahrtanwendungen.
Ein wesentlicher Nachteil von AFCs ist jedoch ihre Anfälligkeit für Kohlendioxid (CO 2)-Vergiftungen. Schon geringe Mengen an CO2 in der Luft (400 ppm) können ihren Betrieb beeinträchtigen und die Reinigung von Wasserstoff und Sauerstoff in der Zelle erforderlich machen. Diese Empfindlichkeit gegenüber CO2 wirkt sich auch auf die Lebensdauer der Zelle aus, d. h. auf die Dauer, bevor sie ausgetauscht werden muss. Nichtsdestotrotz haben AFC-Stacks mehr als 8000 Stunden lang einen stabilen Betrieb gezeigt.
Festoxid-Brennstoffzellen (SOFC) #
Dieser Typ verwendet eine harte, nicht poröse Keramikverbindung als Elektrolyt. Aufgrund der festen Beschaffenheit des Elektrolyten müssen diese Zellen nicht in der für andere Brennstoffzellentypen typischen plattenartigen Konfiguration aufgebaut werden. Es wird erwartet, dass SOFCs einen Wirkungsgrad von etwa 50-60 % bei der Umwandlung von Kraftstoff in Strom erreichen werden.
SOFCs arbeiten bei hohen Temperaturen, ca. 1000 °C. Dieser Hochtemperaturbetrieb macht Edelmetallkatalysatoren überflüssig. Darüber hinaus sind SOFCs die schwefelbeständigste Art von Brennstoffzellen. Sie sind in der Lage, im Vergleich zu anderen Zelltypen deutlich höhere Schwefelmengen zu tolerieren. Sie sind auch immun gegen Kohlenmonoxid (CO)-Vergiftungen, so dass CO als Brennstoff verwendet werden kann.
Die hohe Betriebstemperatur bringt jedoch gewisse Nachteile mit sich. Dies führt zu einem langsamen Start und erfordert eine erhebliche Wärmeabschirmung, um die Wärme zu speichern und das Personal zu schützen. Während dies für Versorgungsanwendungen akzeptabel sein mag, stellt es für Transport- oder kleine tragbare Anwendungen eine Herausforderung dar.
In den letzten Jahren haben sich Protonenaustauschmembran-Brennstoffzellen zur meistgenutzten Technologie für
industrielle Anwendungen im großen Maßstab. Insbesondere die Automobilindustrie hat sich fast
ausschließlich auf dieser Technologie. Das von GRZ Technologies hergestellte DASH Power-System verwendet PEM-Brennstoffzellen.





